
本报告或文章可用于微博、微信公众号、新闻网站等一般性转载,或用于企业的公开市场宣传,或用于企业投融资咨询、上市咨询等用途。这些引用可能是免费的,也可能产生额外的授权费用,头豹将根据您的引用需求向报告或文章发布者取得相应授权,并派专人与您进一步联系。
请务必如实填写引用需求并按授权范围使用本报告或文章,如头豹发现您最终的引用目的超出所引用需求相应的授权范围,头豹有权要求您停止引用并就头豹因此遭受的损失追究您相应的法律责任。

纠错
1. PROTAC:小分子药物研发的新方向
继PD-1、CAR-T之后,全球掀起了PROTAC药物的研究热潮。国内PORTAC药物的研发也在如火如荼开展,从公开信息来看,布局PROTAC技术的公司已超10家,共有5款国产PROTAC创新药步入了临床阶段。近年来罗氏、辉瑞、拜耳、默沙东、GSK、诺华、阿斯利康等制药巨头纷纷加码PROTAC领域。
蛋白在调控人的生理功能中发挥着重要作用,因此成为主要的药物作用靶点。目前的小分子药物开发仅针对了约20%的已知蛋白靶点,约80%的蛋白因缺乏小分子配体而被认为是缺乏成药性的靶点,开发靶向缺乏小分子配体蛋白的创新药物将解决患者迫切的临床需求,极大程度上地拓展新药的发展空间和治疗手段,拥有巨大的市场潜力。
蛋白降解靶向嵌合体(Proteolysis targeting chimera,PROTAC)是一种是基于泛素-蛋白酶解系统而发展的一种通过小分子化合物来诱导实现靶蛋白降解的新技术。传统小分子药物和单抗药物,都需持续占据靶蛋白的活性位点以阻断其功能,属于“占位驱动(occupancy driven)”,这类药物需要满足一定的剂量、足够长的半衰期、足够高的亲和力等条件,易引发副作用大、脱靶毒性和耐药性等问题。而PROTAC只是提供结合活性,触发靶蛋白与E3连接酶结合从而引发降解这一事件,属于“事件驱动(event driven)”,不需要直接抑制目标蛋白的功能活性,药物也不需要与目标蛋白长时间和高强度的结合, 因此可以靶向表面光滑缺乏小分子结合区域的蛋白,及很多无法用小分子调控或抗体无法到达的靶点。
几种典型药物类别体内作用机制的对比分析
数据来源:文献研究,弗若斯特沙利文分析
2. PROTAC实现靶向蛋白降解的作用机理和步骤介绍
PROTAC技术完成靶向蛋白降解的功能是通过泛素-蛋白酶体系统(Ubiquitin-proteasome system, UPS)实现的,UPS是细胞内蛋白质降解的主要途径之一。UPS降解蛋白可以简单地分为三个步骤:首先,由一种连接酶给目标蛋白加上泛素标签;经过多轮泛素化后就有了多个泛素标签;多聚泛素化之后的蛋白会被蛋白酶体识别并被降解。
泛素修饰是一个由3类酶进行的ATP依赖性过程。泛素激活酶(E1)与泛素(Ubiquitin,Ub)形成一个硫酯键,泛素是一种高度保守的76-氨基酸蛋白。这种反应随后可使泛素与泛素结合酶(E2)结合, E2再将泛素传递给相应的泛素连接酶(E3)。E3连接酶可直接或间接地促进泛素转移到蛋白底物上,在泛素羧基端和底物蛋白上的赖氨酸残基之间形成异肽键,或转移到已与蛋白底物相连的泛素上形成多聚泛素链。单泛素化作用包括内吞作用和 DNA 损坏作用,以及亚细胞蛋白定位和转运变化。但是,要将某个蛋白质定位至蛋白酶体进行降解时需要多聚泛素链的多重泛素化循环。蛋白酶体可识别和展开多聚泛素化底物,并将其降解为小肽。这种反应发生在蛋白酶体复合体的柱芯,肽键水解使用核心苏氨酸残基作为催化亲核体。
UPS实现靶向蛋白降解的作用机理
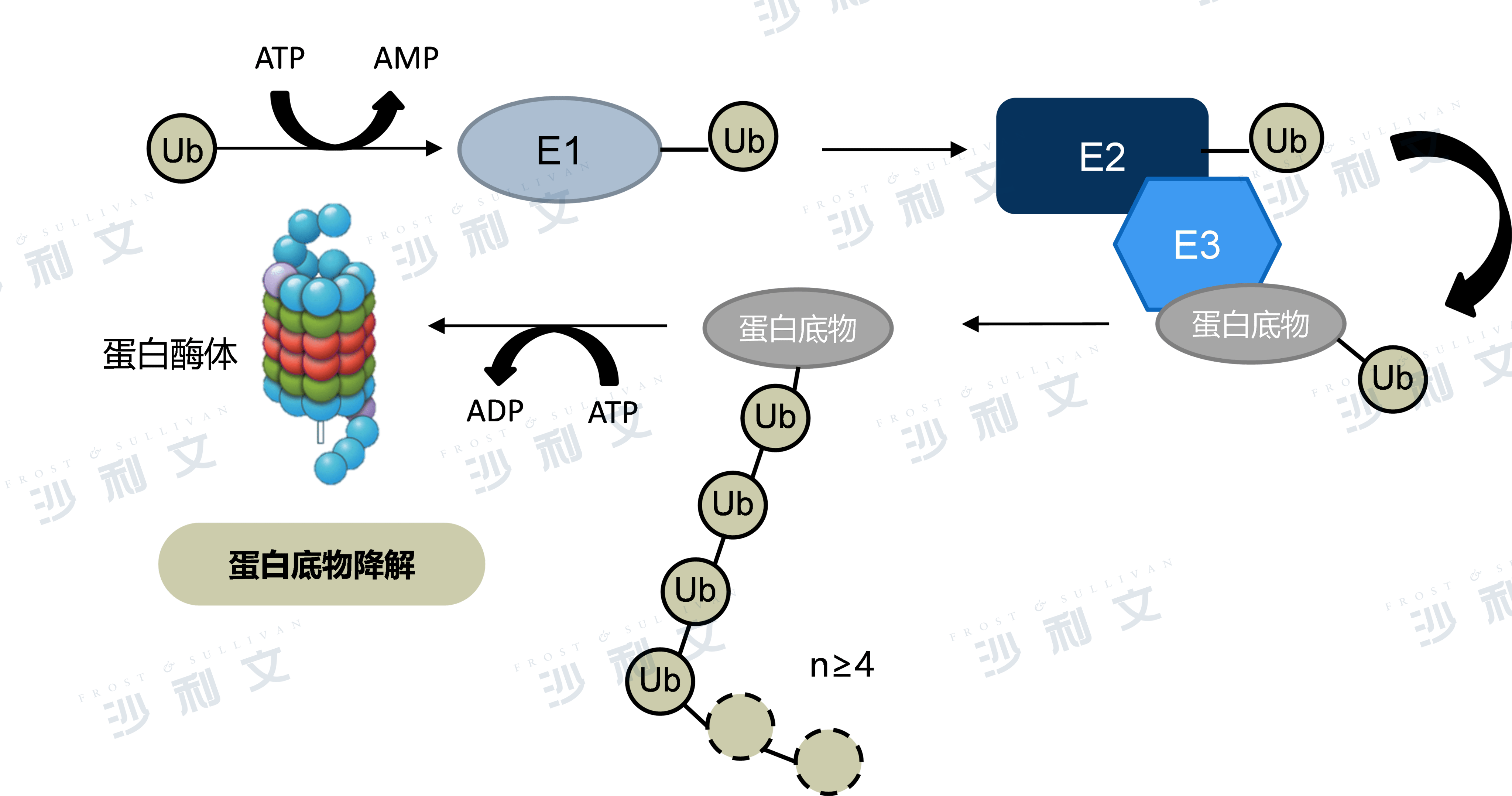
数据来源:文献研究,弗若斯特沙利文分析
3. PROTAC研发历程介绍
2001年,PROTAC概念被最早提出,第一个肽段PROTAC双功能分子被成功地设计和合成出来。2004年,基于VHL的肽段PROTAC被研发出来,但基于肽段的PROTAC被发现活性较低和渗透性差,无法应用到药物开发中。小分子PROTAC最早在2008年被报道出,基于MDM2 E3连接酶的全小分子PROTAC被研发出来。随后2010年,基于cIAP1 E3连接酶的全小分子PROTAC被研发出来,显示出降解CRABP、CRABP II、TACC3、BCR-ABL等功效。自从2015年开始,VHL和CRBN E3连接酶被广泛地运用在全小分子PROTAC的开发中,超过30种全小分子PROTAC被研发和报道出来。基于VHL E3连接酶的全小分子PROTAC被研发出来,并有效地降解了RIPK2、BCR-ABL、BRD4、TBK1等蛋白。基于CRBN E3连接酶的全小分子PROTAC被研发出来,可以靶向BET、FLT3、BTK、ALK、CDK9等蛋白。2019年,Arvinas 公司的2个PROTAC药物,ARV-110和ARV-471,在美国进入临床试验,2020年,BMS的CC-94676也进入临床试验,标志着PROTAC技术的研究进入了新的阶段。
PROTAC技术发展历程和里程碑事件

数据来源:文献研究,弗若斯特沙利文分析
PROTAC技术诞生于2001年,该技术拥有使靶向蛋白泛素化并被降解的功能。自诞生后,PROTAC技术被广泛用于基础生物研究和研究开发,肽段PROTAC和小分子PROTAC先后被设计和合成出来,随着研究的进展,研究者发现了更多E3连接酶的配体,目前共有5个可应用PROTAC的E3连接酶被发现——VHL、MDM2、β-TRCP、cIAP1和CRBN。与此同时,靶点选择也变得更多元化,从雄激素受体(AR)、雌激素受体(ER)、MetAP-2等靶点,到BTK、CDK9、ALK等与癌症进展相关的基因。随着对PROTAC技术和相关机理的了解加深,两个PROTAC候选药物,ARV110和ARV471在美国分别进入I/II期和I期临床试验,这是PROTAC这一类靶向蛋白降解新型药物第一次进入临床试验。
PROTAC技术发展阶段

数据来源:文献分析,弗若斯特沙利文分析
4. PROTAC研发历程介绍
降解靶蛋白的特性使PROTAC分子具有将以前无法成药的蛋白质作为靶蛋白的潜力、在药物耐药中发挥作用以及在除肿瘤外其他治疗领域中拥有治疗潜力的优势。
4.1. 广泛的靶点蛋白和蛋白配体
小分子PROTAC技术具有靶向细胞内疾病靶标的潜力。研究显示,高达80%的蛋白质靶标是传统药物研发手段无法干预的。原因之一是这类蛋白靶点缺乏能够直接参与蛋白功能调节的结合腔。目前小分子药物主要通过与蛋白中的活性结合腔结合,竞争性阻止内源性底物进入结合腔,从而达到阻断蛋白功能的目的。但这种药物研发模式很难应用到缺乏相应结合腔的蛋白中,且对于存在于细胞内部的蛋白,目前也很难开发相应的抗体药物。蛋白质降解可以通过靶蛋白表面上的任何结合位点介导,而不是局限于单个可识别的活性位点,可能更容易开发简单有效和选择性高配体,使没有成药性的蛋白质具有成药价值。
目前,人类蛋白质组中共有600多种E3连接酶(CRBN,VHL,IAP,MDM2,DCAF15,DCAF16,RNF114等),其中只有不到10种被用于开发PROTAC药物。将配体库扩展到具有各种结构特性的E3连接酶,更深入地理解E3连接酶在癌症中的表达谱和必要性,系统地分析其配体性,将进一步扩展PROTAC在化学生物学和治疗癌症中的潜在应用。
4.2. 解决小分子药物的耐药性问题
PROTAC不会出现抑制蛋白时的代偿性增加或突变情况,可以有效地解决耐药性问题。例如PROTAC分子MT-802被验证可以有效克服依鲁替尼产生的耐药性。研究发现,80%的慢性淋巴白血病患者再接受依鲁替尼治疗后都会发生C481S突变,2018年Crew研究组发现MT-802可有效克服这一耐药性。
4.3. 除肿瘤治疗领域的其他领域的治疗潜力
除肿瘤外,PROTAC还有应用于其他治疗领域的潜力。例如在病毒感染领域,NS3蛋白在丙型肝炎病毒(HCV)的感染中起着重要的作用,telaprevir靶向NS3蛋白酶抑制剂治疗HCV被获批,但由于这种抑制剂的低屏障,HCV患者在接受telaprevir治疗后已经形成耐药性,因此telaprevir被撤出市场。一系列创新PROTAC靶向NS3被研发出来,代表性降解物DGY-08-097可以有效降解NS3,不仅包括野生型NS3,也包括NS3突变体。这些结果表明PROTAC技术可用于抗病毒治疗药物的研发。除此之外,PROTAC还被发现潜在用于治疗神经退行性疾病的可能性。Tau蛋白在神经元细胞中起着稳定微管、在蛋白运输中起着提供轨道并维持细胞形态的作用。Tau失调使多种神经退行性疾病的特征,例如阿尔兹海默症(Alzheimer’s disease,AD)和额颞叶痴呆(Frontotemporal dementia,FTD)。针对Tau降解的PROTAC代表性的降解物QC-01-175可以有效降解神经元中的野生型和突变Tau。而且,与健康细胞相比,QC-01-175可以优先降解FTD神经元中的Tau,这些特性和实验结果可为用PROTAC降解Tau来治疗神经退行性疾病提供新的策略。
5. PROTAC研发现状
PROTAC技术的优势明显,该领域的热度也进一步攀升,多家生物技术公司步入该领域,许多大型制药企业也纷纷布局这一技术。
掌握PROTAC技术的龙头企业Arvinas受到诸多大型药企如:默沙东、罗氏、辉瑞、拜耳等公司的重视。2015年,默沙东出资4.3亿美元与Arvinas 达成战略合作。2017年,Arvinas与罗氏/基因泰克扩大了其多年战略许可协议,以涵盖其他疾病目标。 这项合作最初成立于2015年10月,旨在使用Arvinas的PROTAC技术平台开发新的疗法。作为扩展的一部分,Arvinas可获得超过6.5亿美元的开发和商业化里程碑付款,以及产品销售的分级特许权使用费。基因泰克可以选择进一步扩大合作范围,以考虑其他疾病目标。2018年,Arvinas与辉瑞达成研究合作和许可协议,辉瑞可以使用Arvinas专有的PROTAC平台来发现和开发候选药物。2019年,拜耳与Arvinas合作,以利用Arvinas的新型PROTAC蛋白质降解技术为患有心血管、肿瘤和妇科疾病的患者开发新的疗法。此外,拜耳和Arvinas还将联合成立一家新公司,以开发PROTAC技术在农业方面的应用。
Arvinas的战略合作
数据来源:弗若斯特沙利文分析
另一家致力于开发PROTAC技术的Kymera成立于2016年,也同样受到大型企业的关注。2018年,GSK与Kymera达成了长达两年的研发合作协议。2019年,Vertex与Kymera达成了长达四年的合作协议。2020年,赛诺菲与Kymera进行了多计划战略合作,以开发并商业化针对免疫炎症性疾病的同类最先 IRAK4蛋白降解疗法。Kymera将获得1.5亿美金的资金,以及20亿美金的潜在投资金。
Kymera的战略合作
数据来源:弗若斯特沙利文分析
大型医药企业采取投资的的合作方式,进军PROTAC领域,这些企业通过合作来确定该技术在多个领域的治疗潜力。
全球进入临床的PROTAC口服药物已有八款,分别为ARV-110、ARV-471 、CC-94676、CFT7455、KT-474、NX-2127、HSK29116和BGB-16673。目前都处于临床I期或I期/II期的阶段,ARV-110和CC-94676用于治疗转移性去势抵抗性前列腺癌,ARV-471用于治疗乳腺癌。
全球PROTAC药物临床管线
注:竞争格局截至2021年8月31日
数据来源:Clinicaltrials.gov,弗若斯特沙利文分析
在这一波席卷全球的靶向蛋白降解药物开发热潮中,多家中国新药公司出现在国际前沿。此外,多家中国公司也正在布局靶向蛋白降解药物研发平台,数十种药品正在处于临床前研发阶段。
相关推荐
2024年中国元宇宙洞察白皮书:技术突破与模式创新融合发展(独占版)
2024年中国元宇宙洞察白皮书:技术突破与模式创新融合发展
2024年中国元宇宙洞察白皮书:技术突破与模式创新融合发展(摘要版)
2024年中国元宇宙洞察白皮书:技术突破与模式创新融合发展
新能源行业技术发展方向系列研究报告:储能白皮书(摘要版)
目前储能市场中抽水蓄能新增规模第一;电化学储能是现阶段应用范围最广、发展潜力最大的电力储能技术,其中,锂离子电池是电化学储能技术发展的重心。 预计在2025年电化学储能装机量将首次有机会超越抽水蓄能装机量,而飞轮储能和压缩空气储能也将保持较高增速。
新能源行业技术发展方向系列研究报告:储能白皮书(独占版)
目前储能市场中抽水蓄能新增规模第一;电化学储能是现阶段应用范围最广、发展潜力最大的电力储能技术,其中,锂离子电池是电化学储能技术发展的重心。 预计在2025年电化学储能装机量将首次有机会超越抽水蓄能装机量,而飞轮储能和压缩空气储能也将保持较高增速。
2023年中国动力电池行业概览:动力电池创新技术&补能及回收技术分析(摘要版)
动力电池市场持续高速扩张,带动相关产业链蓬勃发展,其补能和回收技术也受到广泛的关注。动力补能技术包括充电和换电技术,是指利用电力在车辆与充电器之间双向流动的技术,控制充电时长和充电速度,以充电桩的形式进行表现。充电桩是指为电动汽车提供充电服务的充能设备,充电桩建设成本低,保有量大,行业运营模式成熟,但充电花费时间长,利用率低。换电是指通过直接替换电能载具的电池来补充电能的一种全新模式,换电站换电速度快,但保有量低,全行业标准化及规模化难度大。动力电池回收是指当动力电池容量随着使用次数的增加而不断降低,不再适用于电动车后,回收废旧动力电池,通过加工处理后进行电池或金属资源二次利用的过程,通常有梯次利用和再生利用两种方式。目前中国动力电池回收仍处于发展的初步阶段。中国目前布局动力电池回收业务的企业数量多、类型杂,多数企业产线达不到满产状态,动力电池回收行业产能闲置现象明显
头豹的程序员小GG强烈建议您使用谷歌浏览器(chrome)以获得最佳用户体验。