
本报告或文章可用于微博、微信公众号、新闻网站等一般性转载,或用于企业的公开市场宣传,或用于企业投融资咨询、上市咨询等用途。这些引用可能是免费的,也可能产生额外的授权费用,头豹将根据您的引用需求向报告或文章发布者取得相应授权,并派专人与您进一步联系。
请务必如实填写引用需求并按授权范围使用本报告或文章,如头豹发现您最终的引用目的超出所引用需求相应的授权范围,头豹有权要求您停止引用并就头豹因此遭受的损失追究您相应的法律责任。

纠错
细胞与基因治疗凭借其可以从根源上治疗疾病、一次性治疗带来长期疗效、对罕见病和难治性疾病提供治疗希望等诸多优势成为当前极具潜力的治疗选择。顾名思义,细胞与基因治疗可以分为细胞治疗与基因治疗。细胞治疗是指应用人自体或异体来源的细胞经体外操作后输入(或植入)人体,用于疾病治疗的过程。体外操作包括但不限于分离、纯化、培养、扩增、活化、细胞(系)的建立、冻存复苏等。目前主要的细胞疗法方式为免疫细胞治疗和干细胞治疗。基因治疗是指通过基因添加,基因修正,基因沉默等方式修饰个体基因的表达或修复异常基因,达到治愈疾病目的的疗法。基因治疗可分为体内基因治疗和体外基因治疗,其中体内基因治疗是指将携带治疗性基因的病毒或非病毒载体直接递送到患者体内,获批药物如2019年经FDA批准的Zolgensma,是一种治疗脊髓性肌肉萎缩症的基于腺相关病毒载体的体内基因疗法。体外基因治疗则指将患者的细胞在体外进行遗传修饰后回输,目前世界最贵的药物正是来自体外基因治疗——Bluebird Bio的Zynteglo,用于治疗因患β-地中海贫血症而需要定期输血的患者。
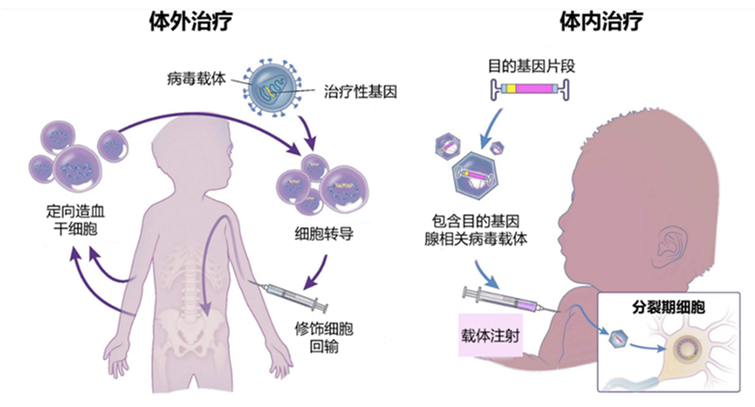
本文将围绕干细胞疗法作重点介绍。干细胞疗法是指把健康的干细胞移植到患者体内,凭借干细胞强大的分化能力,起到修复病变组织或重新构建正常组织的作用。干细胞疗法凭借干细胞多向分化、免疫调节和分泌生长因子等功能,成为具有广阔前景的治疗选择。
造血干细胞
造血干细胞是一类具有自我更新及分化能力的成熟干细胞,有着维持血液系统稳态和再生的能力。造血干细胞作为成体干细胞, 位于造血系统级联的顶端, 存在于脐带血、外周血和成年人骨髓中, 数量少, 是一群具有自我更新能力和全能性的细胞, 能分化为各种类型的造血祖细胞, 进而分化产生不同谱系的骨髓和淋巴样血细胞。在分化过程中, 造血干细胞首先丢失了自我更新能力, 然后逐步失去多向分化的能力, 最终变为具备特定功能的成熟细胞类型, 如红细胞、血小板、粒细胞、DC细胞、B 细胞、T细胞、NK细胞等。
造血干细胞来源于胚胎中胚层的主动脉−性腺−中肾区的动脉内皮细胞, 造血干细胞经血液循环迁移到胎肝, 大约于在孕6周时造血干细胞发生向肝脏的定植,成人阶段则定植到骨髓。在压力环境下造血干细胞也可以迁移到骨髓外进行造血作用。因成熟的血细胞寿命短, 造血干细胞可为血液系统终身补充血细胞。
造血系统是细胞与基因治疗的理想标靶。可对分离得到的造血干细胞进行基因编辑、基因修饰、基因沉默等行为,再回输入体内。造血干细胞的获取方式主要包含传统的骨髓穿刺和目前临床比较常用的血细胞单采术(收集经细胞因子动员的外周血造血干细胞)。使用造血干细胞进行细胞与基因治疗在实际操作过程中也存在不少挑战:比如造血干细胞数量稀少、造血干细胞在体外编辑过程中分化功能可能受损,因此保证造血干细胞在体外编辑过程中功能完整和数量充足是基因编辑的关键。在未来,包括X-连锁严重联合免疫缺陷病、腺苷脱氨酶缺乏性重度联合免疫缺陷症、戈谢病、慢性肉芽肿、获得性免疫缺陷综合征、β-地中海贫血、镰刀状贫血、范可尼贫血等都可能成为基于造血干细胞的细胞与基因治疗的潜在适应症。事实上,基于造血干细胞的细胞与基因治疗已经在治疗β-地中海贫血上有了临床产品——Bluebird Bio的Zynteglo。β-地中海贫血症是指合成血红蛋白的β-珠蛋白基因突变引起的血液性疾病,主要表现为血红蛋白的减少或缺失。Zynteglo则是通过编辑修饰患者的造血干细胞来为每位患者单独制作的。患者自体的造血干细胞在体外被携带β-珠蛋白基因的慢病毒感染,以病毒为载体将β-珠蛋白整合到造血干细胞中,再回输入患者体内。修饰后的造血干细胞通过血液循环系统被运送到骨髓,在那里它们开始产生能表达β-珠蛋白的红细胞和血红蛋白。目前, 针对中型和重型地中海贫血的常规治疗手段是长期除铁和输血, 或者通过合适配型的异体造血干细胞移植来彻底根治地贫疾病。但在实际的实施过程中存在血液资源紧缺和异体造血干细胞配型困难的问题。由此来看,基于患者自体造血干细胞移植的治疗方案不但可以起到对疾病终身治愈的目的, 还可以大大缓解血库压力、节约血液资源。但同时该项治疗方案也存在不少的不足:如高昂的治疗费用、病毒整合β-珠蛋白基因过程中的致癌风险、β-珠蛋白基因表达的稳定性等等。
 干细胞疗法在运动医学上的运用
干细胞疗法在运动医学上的运用
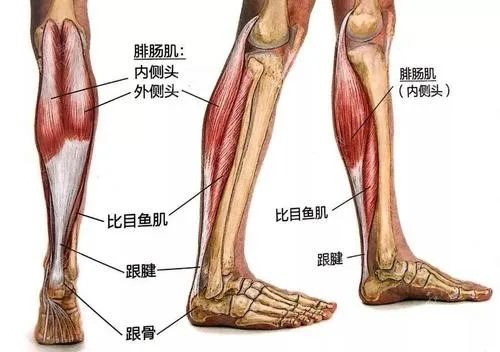
干细胞疗法还可应用于跟腱(肌腱)的修复过程。跟腱是一种肌腱,一端连着足和骨,一端连着两块肌肉(腓肠肌和比目鱼肌)。在高强度的加速、减速、变向、机体疲劳的过程中,跟腱断裂的风险会大。增加。跟腱断裂的恢复过程主要有三个,第一个是发炎,从受伤的时候就开始,一般持续一周左右;第二个是增殖扩散过程,这个过程中III型胶原蛋白会慢慢形成去连接受伤部位,大概持续三周左右;重建过程,III型胶原蛋白慢慢被I型胶原蛋白取代。当肌腱受伤,肌腱内的干细胞就会收到生长因子的信号,进而被释放出来分化为肌腱细胞来修复肌腱,但这是一个非常漫长的过程,干细胞的长时间持续分化可能导致局部的组织增生,且干细胞没有办法完成自身的分裂复制。因此,使用自体或异体的干细胞治疗可以客服这些问题。从外部将提取分离得到的自体干细胞或体外培养得到的异体干细胞注射入肌腱受伤部位,大量干细胞会迅速分化去修复受伤组织。目前干细胞疗法运动医学上有了广泛的运用场景,比如跟腱断裂、韧带断裂等。
随着干细胞疗法在临床上的不断应用,希望未来该项疗法可以从罕见病扩展到更多的慢性病、可以使用更多安全可靠的载体、可以覆盖更广泛的基因,为患者带来更多的治疗获益。
相关推荐
2023年中国EPC细胞药物行业概览
本报告为2023年中国EPC细胞药物行业概览,将梳理当前EPC细胞药物行业的应用情况、临床进展、产业链、发展环境、发展挑战与机遇、竞争格局和标杆企业。
2023年中国免疫细胞存储行业研究报告
本报告为中国免疫细胞存储行业研究报告,将从免疫细胞存储的业务流程出发,通过分析全行业的发展现状以及主要竞争者的参与情况,展开对行业未来发展前景的展望。
2023年中国细胞治疗药物行业白皮书
本报告为2023年中国细胞治疗药物行业白皮书,将通过分析产业链上下游各环节以及各细分行业市场现状,从而研判行业未来发展趋势。
2023年细胞培养肉行业概览
疫情后,传统畜牧业以及人畜关系得到重新审视与广泛讨论,加之环境保护以及动物福利的呼吁,驱动细胞培养肉行业的发展。细胞培养肉全球市场规模2022年达到2.47亿美元,部分企业预计2025年正式投入生产,2025年市场规模预计达到12亿美元,CAGR达到63.41%;根据麦肯锡预测,2030年市场规模将达到200亿美元。处于起步阶段的细胞培养肉行业仍面临诸多挑战,其中政策尚未落实成为进入市场的主要阻碍,其次成本高、消费者接受度低以及技术问题也成为了主要制约因素。
2022年中国干细胞医疗行业研究报告
中国干细胞医疗行业现存发展态势几何,未来剑指何方?
头豹的程序员小GG强烈建议您使用谷歌浏览器(chrome)以获得最佳用户体验。