全文字数:2885字,精读时间:5分钟
本文援引于报告《2021年医药政策系列:MAH(药品上市许可持有人)制度红利释放,引燃医药产业创新热情》,首发于头豹科技创新网(www.leadleo.com)。
头豹科技创新网内容覆盖全行业、深入垂直领域,行业报告每日更新;政策图录、数据工具助您轻松了解市场动态;智能关键词轻松搜索,直奔行业热点内容。
诚挚欢迎各界精英交流合作,头豹承接行业研究、市场调研、产业规划、企业研究、商业计划、战略规划等业务,您可发送邮件或来电咨询。
客服邮箱:CS@leadleo.com 咨询热线:400-072-5588
MAH制度促药品上市许可与生产许可“解绑”,生物医药产研转化升级
药品上市许可持有人制度,即MAH制度(Marketing Authorization Holder),通常指拥有药品技术的药品研发机构、科研人员、药品生产企业等主体,通过提出药品上市许可申请并获得药品上市许可批件,并对药品质量在其整个生命周期内承担主要责任的制度。
自20世纪80年代以来,中国一直实行药品上市许可与生产许可合并的管理模式,2015年MAH制度相关法规政策出台,逐步形成以药品上市许可持有人制度为中心的新制度。MAH制度使得上市许可与生产许可“解绑”,促进生物医药产研转化升级。

MAH制度各省数据揭秘,全面推行一年半后冀京粤三地MAH批准文号最多
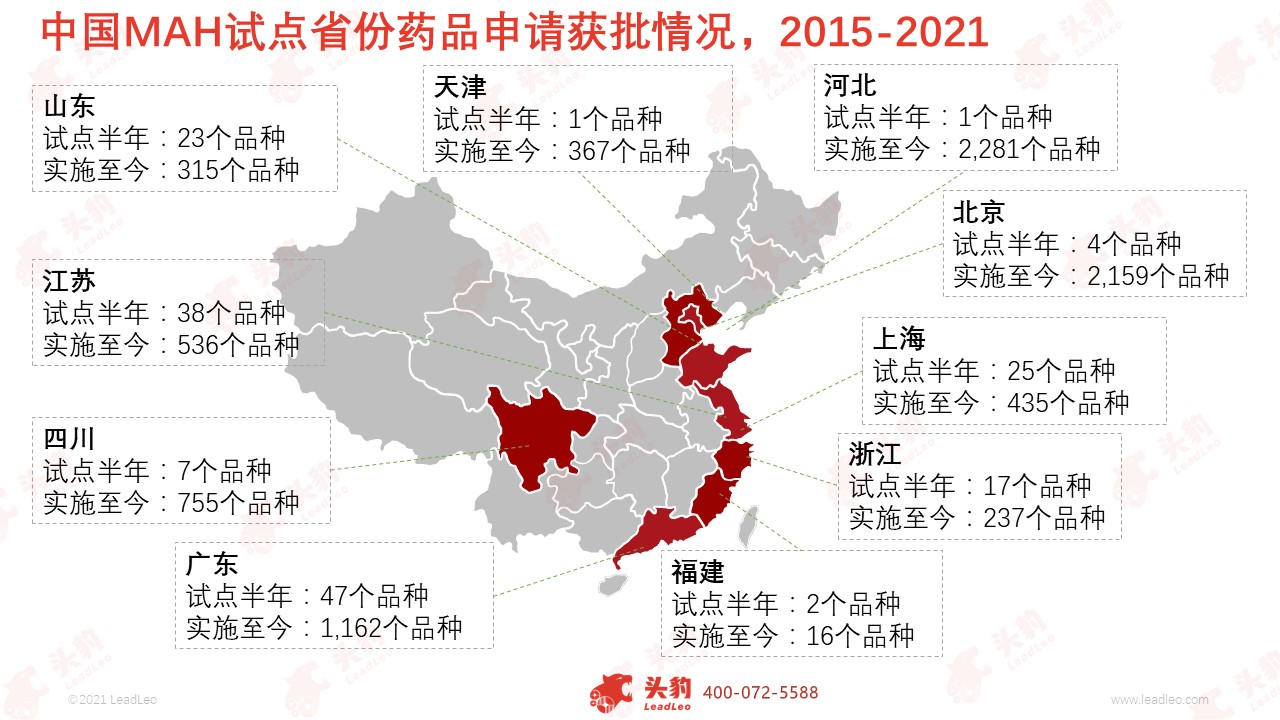
MAH制度十省试点。2015年11月4日,《关于授权国务院在部分地方开展药品上市许可持有人制度试点和有关问题的决定》通过,授权国务院开展药品上市许可持有人制度试点,试点区域包括北京、天津、河北、上海、江苏、浙江、福建、山东、广东、四川十个省、直辖市,原三年期限延长一年至2019年11月。
Insight数据库显示,截至2021年6月按药品批准文号统计MAH品种共25,864个,其中十省市中河北省MAH批准文号数量最多,批准文号涵盖2,281个品种,北京、广东紧跟其后。MAH药品类型上主要以化学药品、中药、生物制品为主,分别为16,981个、8,386个和497个,企业主要分布在河北、北京、广东等地。
试点初见成效,多重利好摸索前进。试点工作开启后,齐鲁制药有限公司的吉非替尼首仿药率先获益,成为首个MAH试点落地品种。该品种的上市可打破进口药企的市场垄断,降低抗癌药物价格,提高国内肺癌患者用药可及性。另外,按照MAH试点方案要求,试点行政区域内的药品生产企业整体搬迁或者被兼并后整体搬迁的,该企业持有药品批准文号的药品可以申请MAH。当时奇星药业厂区属于征拆范围,在政策红利下,奇星药业申请成为公司75个中药品种的MAH,委托其他符合条件的企业进行生产,从而避免处于停产困境。
MAH制度激发药品创新活力,受行业认可推崇
MAH制度避免了药品注册与生产许可“捆绑”模式的弊端。MAH制度改革的意义在于为药品研发的供给端和需求端搭建桥梁,由专业的药品研发企业、科研机构和科研人员开展研发活动,而具有药品生产资质和能力的企业则承担具体的生产功能,旨在推动其存量生产资源供给侧改革,二者分工协同,实现强强联合,从而充分提升制药企业的生产产能利用率,并在一定程度上突破土地资源和环境资源的约束。同时,通过从源头强化研发者责任,生产质量也得到更好提升。
MAH制度受行业推崇。MAH试点工作在众多案例上研究制定出可复制、可推广的制度,参与试点的研发机构和生产企业均认为MAH制度很好保护创新者权益,优化资源整合,加快创新药上市,激发企业活力,促进中国医药产业发展。

MAH制度触及药品专利本质变革,医药行业各领域迎来巨变
MAH制度使得医药市场要素灵活流动,通过实现所有权和生产分离,推动行业CRO、CMO及CSO发展,中国医药生态环境下研发、生产和销售等各领域企业生产关系与市场结构产生巨大变化。
• 对CRO行业影响:MAH实现所有权和生产的分离,激发研发人员积极性,对CRO影响尤为显著。加速本身具备研发能力但不具备生产能力的CRO企业从研发外包服务商转型为专业医药研发机构/制药企业。
• 对CMO行业影响:MAH制度使上市许可与生产许可分离,CMO企业作为受托方快速发展。使得国内的CMO合法化、规范化,持有人的利益能得到保障,越来越多的国内药企会选择和CMO公司进行MAH方面的合作。
• 对CSO行业影响:促进CRO+CMO+CSO上下游不断融合发展,让医药市场要素灵活流动。
• 对传统制药行业影响:MAH有利于生产文号便捷流通,有利于产业结构的调整和资源配置,提高产业集中度,避免重复投资和建设。

MAH制度赋能,CDMO企业MAH业务进入收获期
随着MAH制度的实施,鼓励创新药研发大势所趋,催生未来大量研发外包服务需求,为CXO行业带来巨大的发展机遇。众多知名CDMO公司积极布局创新药MAH业务、I-IV期临床研究等业务,为国内药企提供从临床前研究至药品上市商业化生产、申报文件及现场核查等一站式服务,与国内各大医药企业开展广泛的长期稳定合作,进一步在临床及创新药领域的市场领域拓展,MAH制度的实施促进CXO公司获得新的利润增长点。
合全药业成为中国MAH试点开展以来首个支持获批创新药的受托企业,助力歌礼成功完成原料药的工艺优化、工艺验证和临床报批,并于2017年顺利通过国家药品监督管理局检查。中国首个本土一类抗丙肝创新药物获批上市,MAH制度红利促合作项目快速推进。
作为行业领先的CDMO解决方案提供商,凯莱英深度参与MAH品种开发,首个MAH项目再鼎医药的则乐(尼拉帕利)进入商业化生产,公司全流程服务和黄医药的苏泰达(索凡替尼)2020年底获批上市,推动MAH项目业务进入收获期。

深度见解:医药CXO行业快速发展,借鉴MAH医疗器械注册人制度推行
医药CXO行业快速发展:MAH药品上市许可持有人制度使得医药市场要素灵活流动,中国医药生态环境下研发、生产和销售等各领域企业生产关系与市场结构产生巨大变化。MAH制度使得上市许可与生产许可分离,激发研发人员积极性,对CRO影响尤为显著,CMO企业作为受托方快速发展,药品经营企业及CSO的相关人只要获得MAH授权,就可以进行登记并开展从业活动,促进CRO+CMO+CSO上下游不断融合发展,让医药市场要素灵活流动。
MAH背景下,医疗器械注册人制度全面推行:中国一直以来将药品和医疗器械作为特殊商品实行市场准入制度,并将产品上市许可和生产企业许可按照“双重许可”给予同一主体的“捆绑”模式依法管理。这种“捆绑”模式逐渐暴露出对创新的束缚和对产业链的钳制等问题,一定程度上制约了市场对资源配置的决定性作用,成为医药产业“发展不平衡、不充分”的原因之一。
借鉴药品上市许可持有人制度和国际通行的上市许可持有人(MAH)制度,2017年12月7日《中国(上海)自由贸易试验区内医疗器械注册人制度试点工作实施方案》发布,经过历年来试点范围逐步扩大,2021年3月新版《医疗器械监督管理条例》正式发布,明确全面实施医疗器械注册人制度。
重点关注企业
通过深度研究MAH(药品上市许可持有人)制度,头豹建议重点关注药明康德[603259]、凯莱英[002821]。


