
本报告或文章可用于微博、微信公众号、新闻网站等一般性转载,或用于企业的公开市场宣传,或用于企业投融资咨询、上市咨询等用途。这些引用可能是免费的,也可能产生额外的授权费用,头豹将根据您的引用需求向报告或文章发布者取得相应授权,并派专人与您进一步联系。
请务必如实填写引用需求并按授权范围使用本报告或文章,如头豹发现您最终的引用目的超出所引用需求相应的授权范围,头豹有权要求您停止引用并就头豹因此遭受的损失追究您相应的法律责任。

纠错

2023年11月21日,康乃德公布其对标度普利尤单抗(Dupilumab)的Rademikibart(CBP-201)在中国特应性皮炎患者人群中关键试验的积极长期数据。同日,先声药业宣布已与康乃德就其创新药IL-4Rα单抗Rademikibart订立大中华区的独家许可与合作协议。
康乃德专注于自免领域,利用自身高通量平台构建了具备差异化及高潜力的管线组合,本次康乃德创新药Rademikibart与先声药业的大华区独家许可与合作,将进一步丰富先声药业在自身免疫领域的产品布局,加强自身免疫领域商业化协同效应。
在此背景下,头豹研究院通过对于AD治疗生物制剂Rademikibart关键临床试验结果事件追踪,捕捉事件动向及行业期待,并分析其事件影响,发布了《2023年AD治疗药物行业热点追踪:新一代AD生物制剂渐入佳境》。
热点事件追踪:2023年11月,康乃德公布Rademikibart(CBP-201)在中国特应性皮炎患者人群中关键试验的积极长期数据。Rademikibart在中国针对中重度AD患者的关键试验的第2阶段结果表现优异,16周后能够继续提升疗效,Q2W和Q4W均能提升并维持满意疗效,Q4W方案表现出了同类最佳潜力,安全性表现更佳。
Rademikibart临床试验设计
Rademikibart针对中重度AD患者的关键临床试验(CN002)包括2个阶段,分别为16周的诱导阶段和36周的维持阶段。第一阶段:为期16周,包括随机分配到Q2W Rademikibart(n=219)和安慰剂组(n=111)的患者。第二阶段:为期36周,达到EASI-50(反应者)的患者被随机分配到Q2W Rademikibart(n=113)或Q4W Rademikibart(n=112)组。未达到EASI-50(无反应者)的患者被分配到开放标签的Q2W Rademikibart组(n=86)。患者接受为期36周(至第52周)300mg Q2W或Q4W治疗。
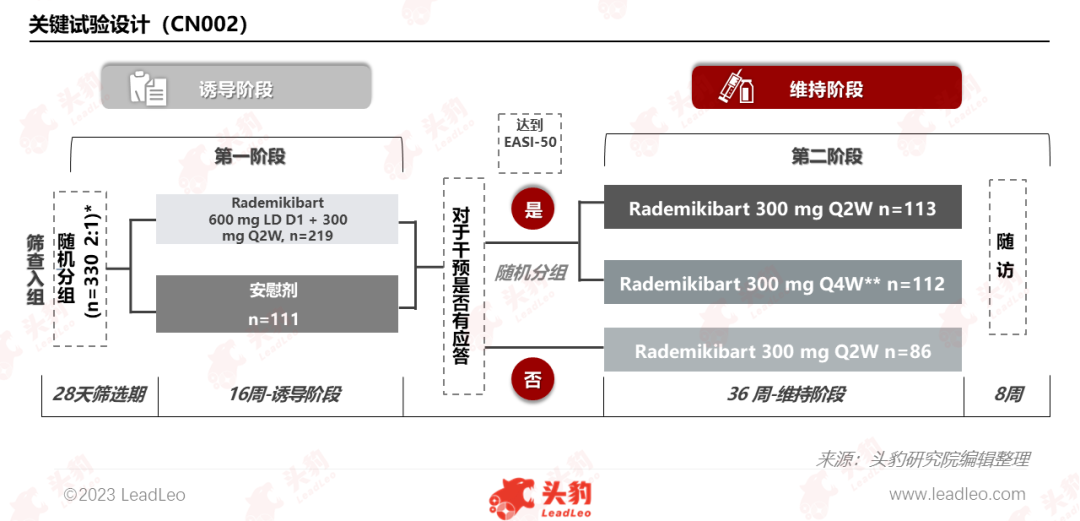
Rademikibart临床试验设计
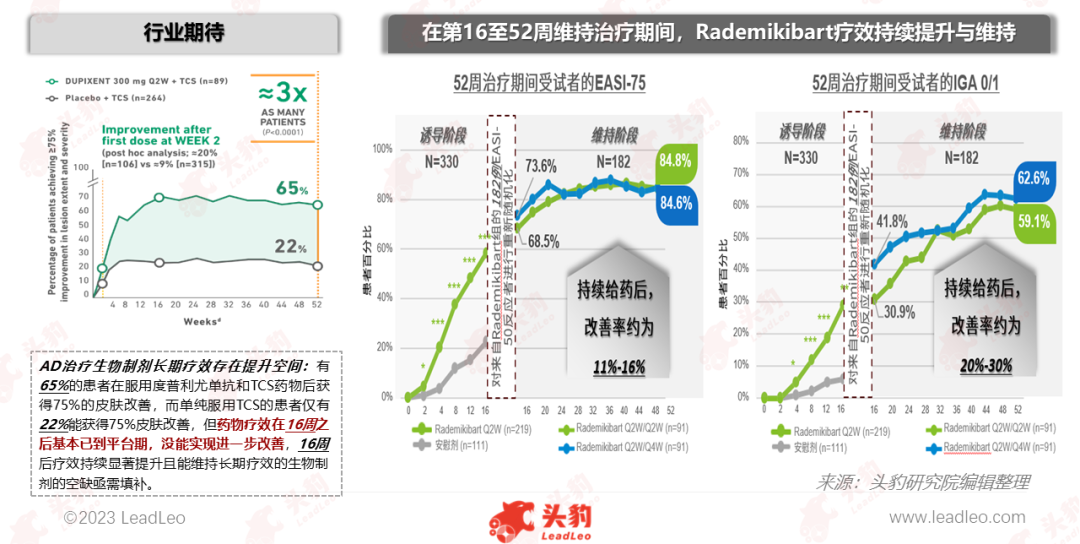
关键发现一:16周后,治疗效果持续改善。
临床试验显示,在第16至52周的治疗过程中,Rademikibart在Q2W与Q4W不同给药方案下都能观察到持续向好的疗效表现。随着维持治疗期间疗效持续改善,长期疗效不断深化,从16周到52周,EASI-75提高一至两成, IGA 0/1提高两至三成,两个方案组的EASI-75分别达到84.8%、84.6%, IGA 0/1分别达到59.1%、62.6%。现有的AD治疗药物在疗效维持方面有待改善,疗效在16周之后基本已到平台期,与目前可用的治疗相比, Rademikibart在维持阶段疗效优势明显。Rademikibart在第16周后疗效的持续提升成为AD生物制剂重大突破,超越同IL-4Rα靶点生物制剂潜力,或将填补AD治疗生物制剂市场现有空缺。
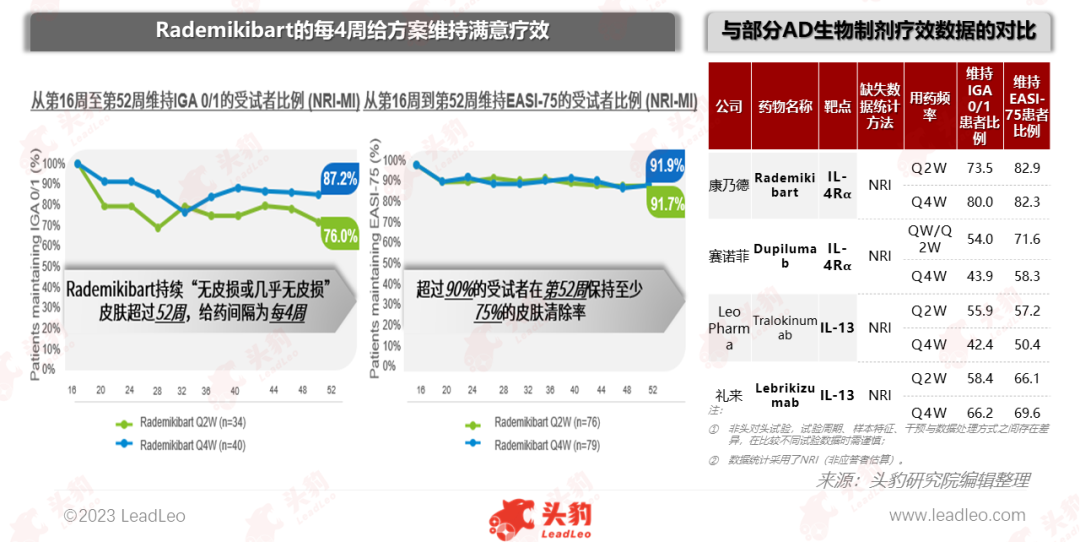
关键发现二:16周后,Q2W和Q4W两种方案均能提升并维持满意疗效,Q4W方案表现出了同类最佳潜力。
临床试验显示,在第16周至第52周期间,对比Q2W与Q4W不同给药间隔,即使给药间隔延长,Rademikibart的Q4W给药方案仍然能够维持较好的疗效。当前的IL-4Rα靶点的AD生物制剂以每2周给药方案为主,可能使患者产生“针头疲劳”;Rademikibart Q2W和Q4W方案均能维持满意疗效,且Q4W同样也显示出了在皮损清除率、疾病严重程度和瘙痒等方面的显著改善。延长给药间隔提高可患者的依从性,并更好地控制病情,减少AD的复发率,有利于AD患者的长期治疗。并可减轻患者和卫生系统负担,提高医疗资源的利用效率。Rademikibart的Q4W给药方案表现出同类最佳潜力,在AD生物制剂领域中具有突破性的潜力。
关键发现三:Rademikibart显示出良好的安全性,在长达52周的长期治疗中没有新的安全信号。
目前的AD治疗药物在安全性方面仍有进步空间,如JAK抑制剂乌帕替尼的安全性分析中显示其导致痤疮发生率升高,芦可替尼对严重感染、恶性肿瘤、主要不良心血管事件进行盒装警告。此外,AD生物制剂结膜炎的副作用也受到较多关注;此次Rademikibart临床试验结果显示出较好的安全性,相比达必妥结膜炎的报告率8.4%,Rademikibart为5.3%~8.2%,不良反应的发生率有所改善,安全性表现更佳。

事件影响
创新药宏观政策概述:中国创新药行业的发展有利于满足广大未满医疗需求、提高医疗水平以及对标国际先进技术水平,因此中国政府高度重视医药创新,在《国家创新驱动发展战略纲要》、《医药工业发展规划》等政策规划中均提出有关创新药发展的目的,大力鼓励发展中国创新药市场的发展。在针对创新药的研发支持政策与审评审批程序影响下,一方面有望激发行业研发热情;另一方面,关门效应约束了部分热门靶点的项目涌入,引导企业在开展创新药研发项目时,在以临床需求为导向的同时权衡市场热度。若进度较快的AD生物制剂率先进入NDA阶段,可能对研发进度处于非头部位置的企业造成较大的进度压力,或需调整适应症方向,导致投入更多研发成本与精力。

中国AD生物制剂市场热度分析:目前中国AD治疗生物制剂市场中,IL-4Rα靶点的相关在研药物较多,但获批者较少,除目前已上市的度普利尤单抗以外,Rademikibart此次临床试验数据显示出优异的临床价值和市场潜力。康乃德与康诺亚作为研发格局的第一梯队企业,其产品进度将对其余市场参与者产生一定压力。

康乃德与先声药业达成商业化合作
Rademikibart的最新临床试验结果所展现的临床价值给予患者以及投资者更多信心,与先声药业的独家许可与合作协议有望推动药物早日面世,提振两方公司市场价值。

康乃德与先声药业达成商业化合作事件解读
先声药业的合作获利与市场关注:Rademikibart有望进一步加强先声药业在免疫疾病的产品组合,形成更有效、差异化的创新药产品矩阵,加强自免领域的商业化协同效应。先声药业在研发、生产、商业化各阶段形成了全面、平衡的布局,在多个领域有着较为丰富的产品管线,此次合作预计能够较快进入商业化阶段,在未来一年内有望看到曙光,较快搭建其盈利点。目前,Rademikibart正面临NDA申报的关键阶段,公司的商业化团队仍需尽早完成申报以及商业化布局。
康乃德的合作获利与市场关注:此次license-out标志着康乃德首次完成从0到1商业闭环,夯实了康乃德全球化布局的基础。这将充实康乃德的现金储备,得以支持其未来开展更多重磅管线的研发。Rademikibart作为目前IL-4Rα单抗巨大蓝海市场中研发进度较快且具有差异化临床优势的项目,有望给予患者及投资者更多信心。中国临床试验数据表现可圈可点,但全球化布局仍需更多海外或国际多中心临床试验数据支撑,同时发展更多重磅自免管线,持续推进研发成果的陆续发布。
Biotech与Pharma合作共赢之道:一款新药从研发到NDA及上市需要全产业链的协作,在面临的产品创新、渠道拓展、经营管理等挑战影响下,Biotech与Pharma的商业化合作有望实现效益最大化,在市场不确定因素下开辟合作共赢之道。Biotech与Pharma的合作将成为中国医药市场重要发展趋势之一。创新药在销售团队搭建、学术推广等上市后商业化推广活动中,具有高投入与高风险,成熟的全球头部药企每年需要拿出20%-30%的销售额用于药品销售推广,这一比例在Biotech中则会更高。因此,Biotech不仅面临创新药研发失败风险,还有因过高的商业化投入所导致的资金链断裂风险。Biotech与Pharma的合作可以规避繁冗的商业化事项,从而更为专注于创新药的研发工作。Biotech与Pharma的商业化合作频发,作为细分赛道专注者的Biotech,拥有更强的靶点化能力、技术平台以及产品创新能力,而作为商业化发展更为成熟的Pharma,则可以在产品的临床研发、申报注册、市场销售方面给予助力,帮助药物快速推进临床实现商业化。在市场竞争加剧、出海战略、国产替代进程加速等影响下,两者的协作创新、合作共赢有望挖掘更多适应症填补市场空白,满足庞大患者需求,推动中国创新药市场走向国际。

本文推荐阅读

《2023年AD治疗药物行业热点追踪》
↓↓长按扫描下方二维码获取↓↓

相关推荐
2024年中国帕金森病药物治疗行业概览: 患病负担全球占比36.5%,治疗方案由多巴胺替代转向精准诊疗前景如何?(摘要版)
帕金森病是由纹状体多巴胺减少和神经元内蛋白异常聚集引发的一种神经系统变性疾病,多数患者无家族病史。根据Hoehn-Yahr分级可将患者分为早期和中晚期,早期用药以运动并发症治疗为主,用药包含多巴胺受体激动剂、MAO-B抑制剂、COMT抑制剂和抗胆碱能抑制剂等,中晚期患者的运动并发症治疗需在早期患者治疗方案基础上对用药疗程和剂型进行调整,另外需考虑患者睡眠障碍、自主神经功能障碍和感觉障碍等非运动并发症,用药包含对症治疗的5-羟色胺在社区抑制剂和甾体抗炎药等。中国帕金森患病负担已接近全球患者的40%,居于全球之首,因此个体用药需求主导的精准诊疗服药方案成为当下药品生产企业和科研机构研发的重点。上世纪末期,全球帕金森药物治疗市场已有多种药品上市,而中国由于科研资源紧张,自研进展较缓,因此用药多依靠海外品牌进口,近年多政府部门颁布利好政策,科研拨款增加的同时,仿制药审评审批政策重点关注临床短缺药品领域,本土在研药物在政策推动下加快商业化脚步,中国用药市场已显现差异化竞争实力。除药物治疗方案外,中科院科研团队目前针对干细胞治疗方案展开研究,以期通过神经细胞再生的方式帮助患者摆脱终身用药的困扰,为中国帕金森治疗市场创造广阔的发展前景。
2024年中国帕金森症药物治疗行业概览:患病负担全球占比36.5%,治疗方案由多巴胺替代转向精准诊疗前景如何(独占版)
帕金森病是由纹状体多巴胺减少和神经元内蛋白异常聚集引发的一种神经系统变性疾病,多数患者无家族病史。根据Hoehn-Yahr分级可将患者分为早期和中晚期,早期用药以运动并发症治疗为主,用药包含多巴胺受体激动剂、MAO-B抑制剂、COMT抑制剂和抗胆碱能抑制剂等,中晚期患者的运动并发症治疗需在早期患者治疗方案基础上对用药疗程和剂型进行调整,另外需考虑患者睡眠障碍、自主神经功能障碍和感觉障碍等非运动并发症,用药包含对症治疗的5-羟色胺在社区抑制剂和甾体抗炎药等。中国帕金森患病负担已接近全球患者的40%,居于全球之首,因此个体用药需求主导的精准诊疗服药方案成为当下药品生产企业和科研机构研发的重点。上世纪末期,全球帕金森药物治疗市场已有多种药品上市,而中国由于科研资源紧张,自研进展较缓,因此用药多依靠海外品牌进口,近年多政府部门颁布利好政策,科研拨款增加的同时,仿制药审评审批政策重点关注临床短缺药品领域,本土在研药物在政策推动下加快商业化脚步,中国用药市场已显现差异化竞争实力。除药物治疗方案外,中科院科研团队目前针对干细胞治疗方案展开研究,以期通过神经细胞再生的方式帮助患者摆脱终身用药的困扰,为中国帕金森治疗市场创造广阔的发展前景。
2024年中国获得性血友病药物治疗行业概览: 近6万人患病,国产药品发展空间如何?(摘要版)
获得性血友病是一种由于妊娠、衰老或恶性肿瘤等基础疾病导致的血液系统疾病,抗凝血因子自身抗体异常产生,导致患者体内凝血因子活性降低,出现无原因出血症状。根据受抑制的凝血因子类型可将患者分为获得性血友病A和获得性血友病B,另外根据患者临床诊疗时出血症状的严重程度,可对症进行止血治疗或免疫抑制治疗。止血治疗一线用药多为凝血因子或凝血酶原复合物,免疫抑制治疗则多选用糖皮质激素联合环磷酰胺进行长期药物调整。当前中国市场已有本土自研的重组凝血因子产品面世,免疫抑制药物方面也有多种仿制药上市过评,本土临床治疗对于进口产品的依赖逐渐降低。面对药物价格过高导致的用药渗透率不足,近年国家医保局重点关注获得性血友病用药的医保支付比例,最大限度为患者减轻药物治疗负担。另外,由于居民对获得性血友病的防控意识不足,部分患者首次并未正确选择就诊科室,导致超三成患者经历延迟确诊。中国获得性血友病诊疗指南提出,对于存在不明原因出血的送诊患者应进行凝血五项检查,根据各项检查结果进一步采取对应的凝血功能测试以尽早实现确诊。本报告将从获得性血友病药物治疗行业的起病原因、用药分类、产业链各环节重点事项分析、市场规模预测及市场竞争格局分析等维度对获得性血友病药物治疗行业进行深度剖析。
2024年中国获得性血友病药物治疗行业概览:近6万人患病,国产药品发展空间如何?(独占版)
获得性血友病是一种由于妊娠、衰老或恶性肿瘤等基础疾病导致的血液系统疾病,抗凝血因子自身抗体异常产生,导致患者体内凝血因子活性降低,出现无原因出血症状。根据受抑制的凝血因子类型可将患者分为获得性血友病A和获得性血友病B,另外根据患者临床诊疗时出血症状的严重程度,可对症进行止血治疗或免疫抑制治疗。止血治疗一线用药多为凝血因子或凝血酶原复合物,免疫抑制治疗则多选用糖皮质激素联合环磷酰胺进行长期药物调整。当前中国市场已有本土自研的重组凝血因子产品面世,免疫抑制药物方面也有多种仿制药上市过评,本土临床治疗对于进口产品的依赖逐渐降低。面对药物价格过高导致的用药渗透率不足,近年国家医保局重点关注获得性血友病用药的医保支付比例,最大限度为患者减轻药物治疗负担。另外,由于居民对获得性血友病的防控意识不足,部分患者首次并未正确选择就诊科室,导致超三成患者经历延迟确诊。中国获得性血友病诊疗指南提出,对于存在不明原因出血的送诊患者应进行凝血五项检查,根据各项检查结果进一步采取对应的凝血功能测试以尽早实现确诊。本报告将从获得性血友病药物治疗行业的起病原因、用药分类、产业链各环节重点事项分析、市场规模预测及市场竞争格局分析等维度对获得性血友病药物治疗行业进行深度剖析。
2024年中国工控行业系列报告(下):企业竞争力排行榜解读,出海市场趋势明显(独占版)
本报告为工业控制行业系列报告第二篇,主要对行业竞争格局进行分析,以及预判未来发展趋势,包括国产替代趋势和出海市场发展趋势。
头豹的程序员小GG强烈建议您使用谷歌浏览器(chrome)以获得最佳用户体验。